系统性红斑狼疮 (systemic lupus erythematosus,SLE) 是一种全身多脏器损伤的自身免疫性炎症性疾病。它常常累及肾脏,带来狼疮肾炎(lupus nephritis ,LN)。
狼疮肾炎(LN)的预后跟肾脏活检表现有很强的关联。根据目前的肾脏病理分类原则,LN 被归入免疫复合物相关肾炎。大体上可以分为 6 个类型,即:
(1)轻微系膜性 LN(Ⅰ型);(2)系膜增生性 LN(Ⅱ型);(3)局灶增生性 LN(Ⅲ型);(4)弥漫增生性 LN(Ⅳ型);(5)膜性 LN(Ⅴ型);(6)严重硬化性 LN(Ⅵ型)。
然而,实际上根据此分类还不足以全面描述 LN 的病理表现。比如:(1)肾小管间质性病变;(2)肾血管病变;(3)肾小球足细胞病变。除此以外,组织学上的急慢性改变也对预后、治疗有重要提示。
由于单纯膜性 LN 跟其他分类的 LN 有较大的不同,所以是我们今天的讨论主题。 (系统性红斑狼疮常常累及肾脏)
(系统性红斑狼疮常常累及肾脏)
1膜性 LN 与其他膜性肾病
除 SLE 的骨骼肌肉痛、皮疹等全身表现外,膜性 LN 肾脏通常表现为大量蛋白尿。相对其他病理类型,膜性 LN 起病相对缓慢、隐匿,且更易带来低蛋白血症。
部分膜性 LN 的其他脏器表现不明显。这导致易误诊为原发性膜性肾病。了解原发性膜性肾病跟膜性 LN 的病理特征则可减少误诊。
跟其他膜性肾病一样的组织病理特征:
(1)光镜表现:所有肾小球均出现毛细血管壁弥漫性增厚,但没有显著的细胞过多。不过很早期,肾小球在光镜下可能看上去完全正常。随着疾病进展到后期,可出现肾小球慢性硬化和肾小管间质改变。
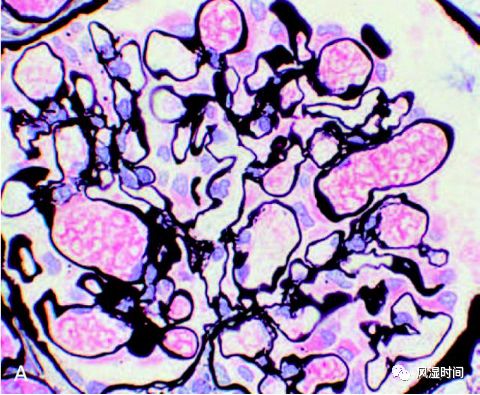
(早期膜性肾病,光镜下完全正常。参考 2)
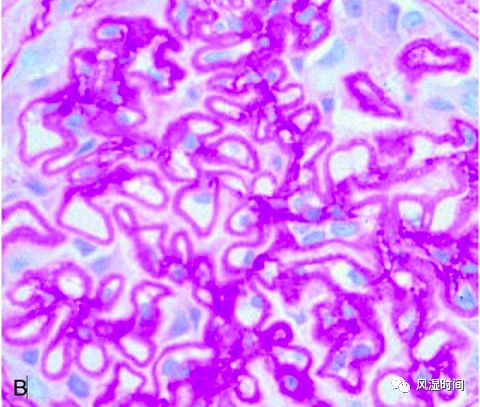
(跟上图同人,出现组织学进展。肾小球毛细血管壁增厚;参考 2)
(2)免疫荧光:可见沿肾小球基底膜的弥漫性颗粒状 IgG 和 C3 染色。
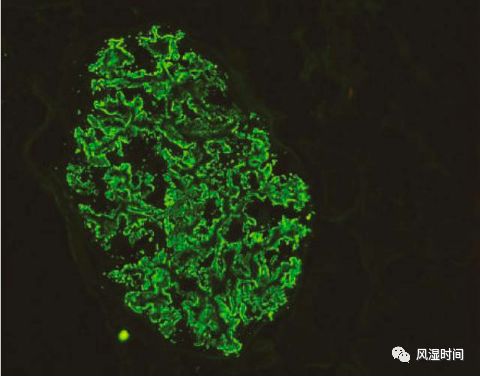
(膜性肾病的 IgG 荧光染色,参考 1)
(3)电子显微镜:刚起病时,上皮下电子致密物沉积在肾小球基底膜外表面;上覆的足细胞足突消失。此后,肾小球基底膜增厚扩张,沉积的电子致密物被融合进基底膜内。
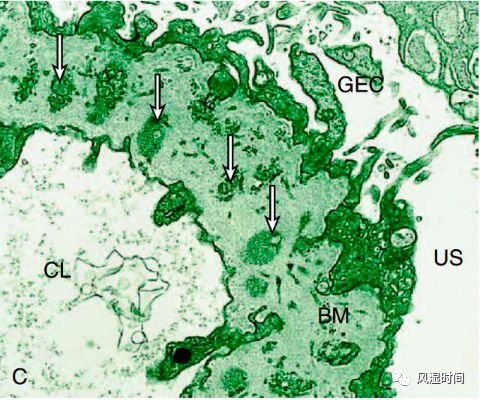
(电子显微镜显示基底膜增厚;箭头指沉积的电子致密物。参考 2)
膜性 LN 跟其他膜性肾病的区别点:
(1)原发性膜性肾病患者的血清里往往有磷脂酶 A2 受体(Phospholipase A2 receptor,PLA2AR)的自身抗体。而且抗 PLA2R 抗体的滴度跟疾病的严重度相关。肾小球免疫病理也可以看到抗 PLA2R 抗体沉积。另一小部分为 1 型血小板反应蛋白 7A 域(THSD7A)抗体阳性。
(2)肾小球内皮细胞中存在网管状结构则强烈提示膜性 LN,而不是原发性膜性肾病。
(3)肾小球外,肾小管基底膜免疫荧光 IgG 染色提示膜性 LN。但原发性膜性肾病很罕见有肾小管免疫荧光染色阳性。
(4)原发性膜性肾病的免疫病理为:上皮下免疫荧光染色显示免疫沉积物主要是 IgG 和 C3。膜性 LN 的表现则同时还有:IgA、IgM、C1q;即「满堂亮」模式。
(5)原发性膜性肾病有肾小球基底膜免疫荧光 IgG 染色阳性。但它主要是 IgG4。膜性 LN 则主要为 IgG1、IgG3。
(6)膜性 LN 还可跟其他类型 LN 共存。这就会同时有其他病理类型。(膜性 LN 跟其他膜性肾病有很多的不同)
2单纯膜性 LN 的流行情况、预后
目前研究发现 10%-20% 的 LN 患者为单纯膜性 LN。
同样偏高的尿蛋白量,跟增生性 LN 比较,「单纯膜性 LN」的预后要好得多。有单纯膜性 LN 的研究显示,其 10 年肾存活率为 72%-98%;一旦「合并增生性 LN」,肾脏预后就明显变差。
不过要注意:随时间推移,原先「单纯膜性 LN」在后来会「合并增生性 LN」。如时间跨度为 10 年,其转变的可能性高达 35%。
这些事实告诫我们:LN 病人应积极肾脏活检。尤其是病情偏重、或者病情恶化时。没有肾脏活检指导,LN 病人的经验性治疗未必恰当。
比如,给「单纯膜性 LN」病人过度治疗而增加副反应。对「膜性+增生性 LN」的治疗不积极,导致预后不良。(流行病学非常的重要)
3单纯膜性 LN 的合理化治疗
原发性膜性肾病会这样做危险分层:
低风险:6 个月的随访期间,蛋白尿持续低于 4 g/d 且肌酐清除率维持正常。
中风险:蛋白尿为 4-8 g/d 并持续 6 个月以上。
高风险:(1)蛋白尿大于 8 g/d 并持续 3 个月;(2)初始时,血清肌酐清除率明显下降;(3)观察的 3 个月内出现血清肌酐清除率显著下降。
低风险人群 5 年内出现肾功能不全风险低于 8%。有相当比例会自愈。所以,通常对低风险人群不予以激素、免疫抑制剂治疗。而是每 3 个月检测尿蛋白量、血清肌酐等。但可予以 ACEI、或者 ARB 治疗。
「单纯膜性 LN」要比「原发性膜性肾病」更危险。一方面是狼疮本身的多脏器损伤,另一方面「单纯膜性 LN」可能会转变(见预后部分)。而且「单纯膜性 LN」是不会自愈的。
基于此,通常采用如下策略治疗单纯膜性 LN。
(1)所有病人都应口服足量羟氯喹、ACEI/ARB 治疗。除非有相关药物禁忌症。
(2)是否使用激素、免疫抑制剂?应首先考虑非肾脏的病情。比如是否有高热、全身骨骼肌肉疼痛等。如有则应积极使用激素、免疫抑制剂。
(3)积极控制血压、血脂;必要时需抗凝治疗。
如 SLE 的其他脏器损伤不严重,单纯膜性 LN 该如何使用激素、免疫抑制剂呢?
(1)如尿蛋白量 ≥ 3.5 g/天。跟其他狼疮肾炎一样激素冲击 3-5 天后,(也有建议不用激素冲击)改每天口服激素 0.5 mg/kg 治疗,并优先联合吗替麦考酚酯治疗。
(2)如尿蛋白量<3.5 g/天,但 ≥ 1 g/天。则每天口服激素 0.5 mg/kg 治疗。暂不考虑联合免疫抑制剂。
(3)如尿蛋白量<1 g/天。不用激素、免疫抑制剂。除非有其他脏器明显损伤。
上述治疗持续 2 到 3 个月后评估病情。如尿蛋白量低于 1 g/天,或者尿蛋白量下降超 50%。则可以规律减量激素。
上述治疗 2 到 3 个月后,尿蛋白量没有下降超 50% 且还高于 1 g/天,则考虑利妥昔单抗治疗。
既往曾优先考虑使用环孢素、他克莫司来治疗膜性肾病。但是,环孢素等有慢性肾毒性,增加心脑血管疾病远期风险。从长远来看,这不是好的选择。
今年 7 月,NEJM 上发表了《Rituximab or Cyclosporine in the Treatment of Membranous Nephropathy》。研究显示,治疗原发性膜性肾病时,利妥昔单抗显著优于环孢素。利妥昔单抗很可能成为原发性膜性肾病(中、高危病人)的标准治疗方案。
综合目前已有的多个研究,单纯膜性 LN 病人也应更积极使用利妥昔单抗治疗。而不是选择环孢素、他克莫司。(单纯膜性狼疮肾炎需要合理化的诊疗)
参考资料:1.《Oxford Textbook of Clinical Nephrology》(第 4 版)2.《Comprehensive Clinical Nephrology》(第 6 版)3. Uptodate 临床顾问4.Fernando C. Fervenza.《Rituximab or Cyclosporine in the Treatment of Membranous Nephropathy》,N Engl J Med 2019; 381:36-46
首发 | 风湿时间
编辑 | 徐德宇
题图及插图 | 站酷海洛、参考文献
投稿及合作 | xiaospring@163.com
